Lorsqu'une prothèse de genou ou même de dent échoue, que ce soit en raison d'une détérioration, d'une instabilité, d'infections ou d'une réponse inflammatoire de l'organisme, le patient doit souvent retourner à la table d'opération. En plus du coût élevé et de l'inconfort pour les personnes impliquées, ces procédures ont tendance à avoir des taux de réussite inférieurs à ceux des chirurgies primaires et génèrent des impacts économiques indirects, tels que des arrêts de travail et une perte de productivité.
Face à ce scénario, la chercheuse Mayara Carla Uvida a développé, au cours de son doctorat à l'Institut de Chimie (IQ) de l'Unesp, à Araraquara, un revêtement hybride multifonctionnel pour implants métalliques. Le matériau est capable de prévenir la corrosion des prothèses, d'inhiber l'action des bactéries, en plus de favoriser l'adhésion des cellules osseuses, ce qui améliore l'intégration dans l'organisme.
« Quand nous parlons de biomatériaux et d'implants, les interactions avec notre corps commencent à la surface. C'est la surface qui entre en contact avec des fluides biologiques, des cellules, des protéines et des bactéries. Même si le matériau interne est résistant, c'est la surface qui dictera les premières réponses de notre corps à l'implant », explique le scientifique.
Comment la recherche a été développée
Le développement de ce revêtement a nécessité une combinaison de chimie des matériaux, d'ingénierie de surface et de tests biologiques. Pour que ce revêtement (film) agisse sur le métal sans se détacher ou se dégrader rapidement à l'intérieur du corps, la première étape consistait à préparer le titane, en éliminant les impuretés et l'oxyde naturel qui se forme lorsque le métal entre en contact avec l'air. Ceci garantit une surface « propre » pour recevoir le revêtement.
Cette première étape franchie, le titane était prêt à recevoir le film hybride développé tout au long du doctorat. Ce revêtement est composé de deux couches. Le premier contient un matériau déjà utilisé dans les lentilles intraoculaires et les prothèses – un polymère (PMMA – polyméthylméthacrylate) associé à de la silice, un composant inorganique biocompatible et chimiquement stable. Selon Mayara, l'union de ces deux matériaux confère au revêtement une structure dense, à faible porosité, ainsi qu'une adhérence extrêmement élevée à la surface métallique, agissant comme une barrière presque imperméable à la corrosion.
La deuxième couche, plus superficielle, a reçu l'incorporation de phosphates de calcium tels que l'hydroxyapatite et le phosphate bêta-tricalcique, chimiquement similaires aux minéraux osseux, en plus du phosphate d'argent, responsable de la libération contrôlée d'ions à action antibactérienne. De cette manière, le revêtement favorise l’intégration au tissu osseux et empêche la formation de colonies bactériennes.
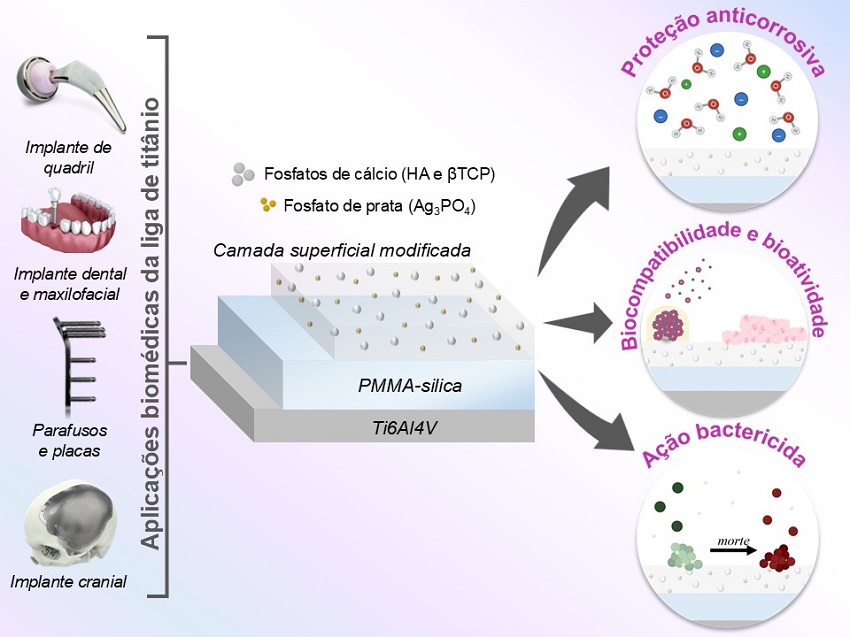
Selon Mayara, pour arriver à cette composition, différentes formulations ont été testées avec des variations de concentrations et de combinaisons d'additifs. «Les meilleurs résultats sont précisément venus des compositions combinant des phosphates de calcium et du phosphate d'argent, une combinaison qui a permis d'obtenir à la fois une bonne réponse cellulaire et une activité antibactérienne», dit-il.
Selon Peter Hammer, professeur à l'Institut de chimie de l'Unesp et conseiller de Mayara, le revêtement représente une avancée pertinente pour le domaine des biomatériaux. « La prévention des infections et des échecs prothétiques est un facteur déterminant pour réduire les reprises chirurgicales et améliorer la qualité de vie des patients, ce qui rend ce type d’approche très prometteur », déclare-t-il.
Du laboratoire à la culture cellulaire
Après leur production, les revêtements ont subi une série de tests impliquant à la fois une caractérisation physico-chimique et une évaluation biologique. En laboratoire, des techniques telles que la spectroscopie des rayons X, la diffraction des rayons X et différents types de microscopie ont été utilisées pour vérifier la composition, la morphologie et l'épaisseur du revêtement, en plus de mesurer son adhérence et sa rugosité. Parmi les tests les plus importants figurait la spectroscopie d'impédance électrochimique, utilisée pour évaluer la résistance à la corrosion de solutions simulant des fluides corporels, car l'environnement interne de l'organisme est riche en ions et peut accélérer les processus de dégradation des métaux.
Ces analyses complètent un ensemble d'études biologiques réalisées en collaboration avec d'autres laboratoires. La partie liée à l'interaction avec les cellules ostéoblastiques, responsables de la formation du tissu osseux, a été réalisée à l'Université Laval, au Canada, où le chercheur a effectué un stage doctoral sous la direction du professeur Diego Mantovani. Là, elle a eu accès à une infrastructure spécifique pour les tests de biomatériaux. Les tests microbiologiques, axés sur l'évaluation de la formation de colonies bactériennes, ont été réalisés à Paraná, dans une installation appartenant au professeur Mantovani dans le parc scientifique et technologique Biopark. Ces tests ont permis de mesurer l'action du phosphate d'argent sur des bactéries courantes, comme Escherichia coli et Staphylococcus aureus.
Selon les chercheurs, cette étape nécessitait une quantité importante d’échantillons, non seulement pour assurer la répétabilité des tests, mais aussi parce que les tests biologiques nécessitent un grand nombre de répétitions pour que les résultats aient une validité statistique.
« Mayara s'est vraiment dévouée. Malgré un doctorat en chimie, le travail nécessitait une approche multidisciplinaire, ce qui l'obligeait à approfondir le domaine biologique pour faire avancer les tests », souligne le professeur Hammer.
Du banc au patient
Malgré des résultats encourageants, le revêtement est encore dans la sphère du laboratoire et il reste un long chemin à parcourir entre un prototype validé et un produit utilisable en milieu clinique. Cette transition passe par différentes étapes, qui impliquent des tests à plus grande échelle, des études complémentaires sur les mécanismes d'interactions biologiques, des essais précliniques et cliniques, en plus des exigences réglementaires imposées par les organismes de santé. Aucune de ces étapes n’avance habituellement sans la participation active de l’industrie, ce qui représente un défi majeur, selon le professeur Hammer.
Un point favorable de cette approche est que la technologie utilise des matériaux relativement accessibles et des procédés simples, ce qui tend à la rendre compétitive si elle passe à des étapes plus appliquées.
« La tendance est à la poursuite de la croissance du domaine des biomatériaux, en se rapprochant d'autres disciplines et en consolidant progressivement les ponts entre le laboratoire et le système de santé », s'interroge le professeur Hammer.